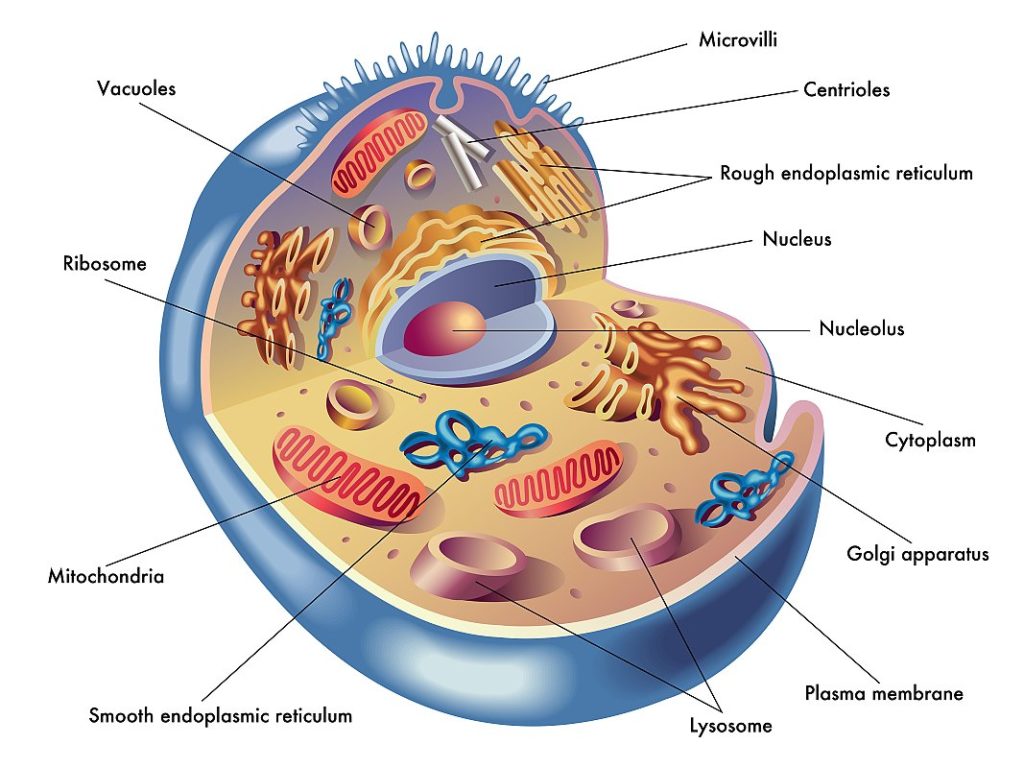
Mitochondrie
Každá buňka v lidském těle je nabitá drobnými organelami nazývanými mitochondrie. Mitochondrie jsou často označovány jako intracelulární motory, protože produkují většinu energie, kterou tělo používá. Buňky s vysokou rychlostí metabolismu, jako jsou buňky srdečního svalu, mohou být vybaveny tisíci mitochondrií, zatímco jiné buňky mohou obsahovat jen několik desítek.
Výroba mitochondriální energie je absolutní nezbytností pro fyzickou sílu, energii, vytrvalost a samotný život. Dokonce i nejmenší pokles výkonu mitochondrií, bez ohledu na to, jak jemný je, může vést k slabosti, únavě a kognitivním potížím. Bohužel, v průběhu stárnutí mitochondriální funkce – stejně jako všechno ostatní – se stávají méně efektivní.
Mitochondriální výroba energie
Produkce mitochondriální energie se uskutečňuje dvěma úzce spojenými metabolickými procesy:
- cyklem kyseliny citronové (také známý jako Krebsův cyklus nebo cyklus trikarboxylové kyseliny) a
- oxidační fosforylací (OXPHOS).
Cyklus kyseliny citronové přeměňuje biologické palivo (uhlohydráty a tuky) na adenosintrifosfát (ATP). ATP je hlavním zdrojem buněčné energie.
Další proces – oxidační fosforylace (OXPHOS) – spojuje vodík s kyslíkem za vzniku ještě větších množství ATP. OXPHOS generuje asi desetkrát více ATP než cyklus kyseliny citronové. Oxidační fosforylace je primární energetický proces pro všechny aerobní organismy.
Mitochondriální oxidační fosforylace (OXPHOS) poskytuje více než 80 procent ATP používaných našimi buňkami pro energii. OXPHOS pracuje velmi efektivně – téměř na 70 procent. To je v porovnání s asi 10 procenty u motorů s vnitřním spalováním a asi 40 procenty u palivových článků na bázi vodíku a kyslíku používaných v kosmických lodích opravdu efektivní.
OXPHOS pracuje přes řetězec elektronového transportu – řetězec pěti proteinových komplexů zabudovaných do vnitřní membrány mitochondrií. Tyto komplexy zahrnují:
- Komplex I (NADH dehydrogenáza)
- Komplex II (sukcinát dehydrogenáza)
- Komplex III (reduktáza cytochromu)
- Komplex IV (cytochrom-oxidáza)
- Komplex V (ATP syntáza)
Oxidační fosforylace přeměňuje adenosin difosfát (ADP) na adenosintrifosfát (ATP) – měnu chemické energie buňky, která může být poté transportována tam, kde je třeba pracovat.
Změny týkající se věku v mitochondriální funkci – příčina stárnutí?
Účinnost produkce a funkce mitochondriální energie klesá s věkem. Důkazy naznačují, že mitochondriální dysfunkce je základem mnoha běžných onemocnění souvisejících s věkem, včetně Parkinsonovy nemoci, Alzheimerovy nemoci, srdečních onemocnění, únavových syndromů a mnoha genetických stavů.
Dr. Christoph Richter ze Švýcarského federálního technologického institutu Zurich napsal:
Snížení oxidativní fosforylační kapacity vede ke snížení očekávané délky života (1995)
Změny, ke kterým dochází při stárnutí v mitochondriích, zahrnují:
- poškození mitochondriální DNA volnými radikály
- snížená účinnost Krebsova cyklu
- pozměněná odezva na dlouhodobé energetické nároky
- porucha dýchacího řetězce v důsledku změn enzymů
- snížení membránové tekutosti
Mitochondrie zdravých mladých dospělých reaguje odlišně na zvýšené požadavky na energii než mitochondrie starších lidí. Mitochondrie mladistvých lidí se přizpůsobuje zvýšeným energetickým požadavkům rychlým množením a regenerací. To vede k tomu, že více mitochondrií produkuje více ATP pro energii. Nicméně, jak stárneme, naše mitochondrie se replikují méně snadno. To znamená, že k produkci energie existuje méně mitochondrií . Méně mitochondrií se pokusí reagovat na zvýšený požadavek hypertrofováním (zvětšováním velikosti). Bohužel tyto větší mitochondrie jsou méně funkční a produkují více škodlivých volných radikálů než jejich mladší, početnější a menší předkové.
Tyto změny mitochondriální účinnosti a funkce jsou přinejmenším částečně spojeny se změnami koncentrace a účinnosti prvků respiračního řetězce. Většina studií svědčí o poklesu počtu komplexů I (NADH dehydrogenasa), II (sukcinát dehydrogenázy) a IV (cytochrom-oxidázy). Navíc, s tím, jak se množství mitochondriálních enzymů mění s věkem, zvyšuje se množství buněk, které zcela postrádají cytochromoxidázu.
Volné radikály jako příčina mitochondriálního stárnutí
Dr. Denham Harman nejprve navrhl mitochondriální dysfunkci jako základní příčinu nemoci související se stárnutím a věkem v roce 1972.
Teorie se obecně soustřeďují na možné mechanismy, kterými mitochondrie mohou být dysfunkční a přispívat ke stárnutí a nemoci související s věkem: např. citlivost mitochondriální DNA na poškození volnými radikály.
Jedinečná vlastnost mitochondrií spočívá v tom, že mají vlastní DNA (kyselina deoxyribonukleová). DNA je látka, ze které jsou vytvářeny geny a chromozomy. Mitochondriální DNA (mtDNA) je zcela odlišná od jaderné DNA (nDNA) v několika ohledech. Nejprve mtDNA není spojena s histony. Histony jsou pozitivně nabité skladovací proteiny, kolem kterých je navíjena jaderná DNA (jako vlákna na cívce), které jsou nezbytné pro ochranu DNA. MtDNA postrádá tento ochranný mechanismus. Za druhé, většina komplexních mechanismů oprav DNA, které opravují poškození jaderné DNA, chybí v mitochondriích. Proto mtDNA postrádá ochranné a opravné mechanismy.
Mitochondriální DNA (mtDNA) se nachází v mitochondriální matrici, v blízkosti vnitřní mitochondriální membrány (kde se produkují jak energie, tak volné radikály). Vzhledem k tomu, že mtDNA neobsahuje ochranné proteiny, je ještě citlivější vůči napadení volnými radikály.
Mitochondriální dysfunkce začíná méně než dokonalým elektronovým transportním systémem. Dokonce za ideálních podmínek unikají z elektronového transportního řetězce některé elektrony. Tyto úniky elektronů interagují s kyslíkem a vytvářejí superoxidové radikály. Vzhledem k tomu, že mtDNA je blízká místu výroby superoxidových, hydroxylových nebo perhydroxylových radikálů a protože postrádá ochranné a opravné mechanismy, je vysoce citlivá na odstranění (poškození) mtDNA vyvolanou volnými radikály. Ve skutečnosti relativně nechráněná a neopravená mtDNA trpí více než desetinásobkem poškození, které tvoří jaderná DNA.
Bohužel, s mitochondriální dysfunkcí může dojít k výraznému zvýšení úniku elektronů a vzniku začarovaného cyklu. Tyto elektrony (volné radikály) mohou poškodit mitochondriální membránu, což vede ke ztrátě fluidity membrány a ke změně její propustnosti. To může vést k další mitochondriální dysfunkci, narušení produkce buněčné energie a zrychlení buněčného stárnutí.
Poškození lipidového peroxidu v mitochondriálních membránách se zvyšuje lineárně a mutace mtDNA se exponenciálně zvyšují s věkem. Barrientos spekuloval, že změny membránové lipidové kompozice by mohly být příčinou snížené membránové tekutosti související s věkem.
Přístupy k regeneraci stárnoucích mitochondrií
Pochopení navržených mechanismů, kterými mitochondriální dysfunkce mohou přispět k nemoci související s věkem a stárnutím, naznačuje několik potenciálních intervencí. Jedná se o:
- zachování optimálního účinku Krebsova cyklu a respiračního řetězce
- obnovení fluidity mitochondriální membrány
- snížení aktivity škodlivých radikálů.
Mnoho živin hraje nepostradatelnou roli v produkci mitochondrií a poskytuje zásadní antioxidační ochranu proti volným radikálům generovaným oxidační fosforylací. Bylo prokázáno, že látky uvedené v tabulce mají obecně pozitivní účinky na stavy spojené s mitochondriální dysfunkcí v řadě studií na zvířatech i na člověku. Tyto látky zmírňují řadu onemocnění vyvolaných mitochondriální disfunkcí, včetně Parkinsonovy choroby, diabetu a únavy. Rostoucí počet lékařů a vědců se domnívá, že živiny podporující mitochondrie se mohou ukázat jako užitečné pro mnoho příznaků spojených se stárnutím a nemocemi souvisejícími s věkem.
Některé mitochondriální bioenergetické zesilovače
- Vitamín B1
- Vitamín B2
- Vitamín B3 (Niacinamid)
- Vitamín C
- Vitamín E
- Vitamín K
- EDTA
- Koenzym Q10
- Idebenone
- Sukcináty
- Dichloracetát
- Acetyl-L-karnitin
- L-karnitin
- PBN
- N-acetyl-cystein
- Kyselina lipoová
- Cvičení
- Ginkgo Biloba
- D-Ribose
- Kreatin
- Taurin
- Omega-3 mastné kyseliny
2. Richter, C. Oxidative damage to mitochondrial DNA and its relationship to aging. Int J Biochem, Cell Biol, 1995,27:7, pp647-653
3. Papa, S. Mitochondrial oxidative phosphorylation changes in the life span. Molecular aspects and physiopathological implications. Biochimica et Biophysica Acta, 1996),87- 105
4. Cortopassi, G., and Wong, A. Mitochondria in organismal aging and degeneration, Biochimica et Biophysica Acta, 1999, 1410: 183-193
5. Harman, Denham. The Biologic Clock: the Mitochondria? J Am Geriatr Soc, 1972,20: 145-147
6. Miquel J, Economos AC, Fleming J and Johnson JE. Mitochondrial role in cell aging. Exp Gerontol 15: 575-91, 1980
7. Miquel J. An integrated theory of aging as the result of mitochondrial DNA mutation in differentiated cells. Arch Gerontol Geriatr 12: 99-117, 1991
8. Miquel J. An update on the mitochondrial-DNA mutation hypothesis of cell aging. Mutation Research 275: 209-16, 1992
9. Zs.-Nagy, Imre. A membrane hypothesis of aging. J Theor Biol, 1978,75: 189-195
10. Zs.-Nagy, Imre. The role of membrane structure and function in cellular aging: a review. Mech Aging Dev, 1979,9: 237-246
….další
11. Zs.-Nagy, I., Ohta, M., and Kitani, K. Effect of centrophenoxine and BCE-001 treatment on the lateral diffusion and constant of proteins in the hepatocyte membrane as revealed by fluorescence recovery after photobleaching in rat liver smears. Exp Gerontol, 1989, 24: 317-330
12. Zs.-Nagy, Imre. The horizons of an interdisciplinary synthesis in experimental gerontology. Arch Gerontol Geriatr, 1991, 12: 329-349
13. Dean, W., Imre Nagy, Antiaging Pioneer, Vitamin Research News 2001: Vol. 15-2
14. De Grey, A. The Mitochondrial Free Radical Theory of Aging, R.G. Landes, Austin, Texas, 1999
15. De Grey, A. Reductive Hotspot Hypothesis of Aging, R.G. Landes, Austin, Texas, 2001
16. Shigenaga MK, Hagen TM and Ames BN. Oxidative damage and mitochondrial decay in aging. Proc Natl Acad Sci USA 91: 10771- 78, Nov 1994.
17. Barrientos, A., Casademont, J ., Cardellach, F ., et al. Qualitative and Quantitative changes in skeletal muscle mtDNA and expression of mitochondrial-encoded genes in the human aging process, Biochemical and Molecular Medicine, 1997, 62: 165-171.
Zdroj: warddeanmd